Na początku marca media obiegła informacja o kolejnym, drugim już przypadku całkowitego wyleczenia zakażenia wirusem HIV. Ze względu na to, że jest to informacja tyleż przełomowa, ile sensacyjna, o jej wyjaśnienie poprosiliśmy dr hab. Monikę Bociągę-Jasik z Katedry Gastroenterologii, Hepatologii i Chorób Zakaźnych UJ. Czy mamy do czynienia z rewolucją w walce z wirusem HIV?
Od 1981 roku, kiedy to w dużych miastach Stanów Zjednoczonych stwierdzono wśród młodych, dotychczas zdrowych mężczyzn, mających kontakty seksualne z innymi mężczyznami (MSM) liczne przypadki zachorowania na pneumocystozowe zapalenia płuc (wywołane przez grzyba Pneumocystis jiroveci) i mięsak Kaposiego (nowotwór tkanek miękkich), dokonał się ogromny postęp w leczeniu zakażenia HIV. Już dwa lata po wykryciu wirusa, w roku 1985 roku podjęto pierwsze próby terapii z zastosowaniem zidowudyny (ZDV – lek antyretrowirusowy stosowany przy zwalczaniu zakażeń wirusem HIV).
Po krótkim pilotażu i badaniu z podwójną ślepą próbą obejmującym zaledwie 282 pacjentów, ZDV zostaje szybko zaakceptowana przez autorytety medyczne i po dwóch latach wprowadzona na rynek. Niestety wkrótce okazuje się, że – w związku z szybkim rozwojem oporności HIV na ZDV – przyjęta strategia terapeutyczna z zastosowaniem jednego leku antyretrowirusowego jest postępowaniem nieskutecznym. Dopiero lepsze poznanie mechanizmów replikacji HIV w kolejnej dekadzie skutkuje odkryciem nowych grup leków antyretrowirusowych i zastosowaniem w 1996 roku leczenia skojarzonego (HAART – Highly Active Antiretroviral Therapy), pozwalającego na kontrolowanie zakażenia i zahamowanie jego progresji.
„Pacjent berliński” – pierwszy zwycięzca w walce z HIV
 Obecnie zakażenie, w przypadku wczesnego wykrycia i wprowadzenia terapii, jest traktowane jako choroba przewlekła, a czas przeżycia pacjentów jest porównywalny do czasu przeżycia ogólnej populacji. Niestety, pomimo bardzo skutecznego leczenia antyretrowirusowego, do tej pory nie udało się nam konwencjonalnymi metodami doprowadzić do eliminacji wirusa z organizmu. Co więcej, nieustanna produkcja nowych cząsteczek HIV, utrata integralności błon śluzowych przewodu pokarmowego i związana z tym ekspozycja na florę jelitową, doprowadzają do stałej aktywacji układu immunologicznego. W efekcie osoby zakażone HIV cechują się zwiększonym ryzykiem wystąpienia m.in. chorób sercowo-naczyniowych i nowotworowych.
Obecnie zakażenie, w przypadku wczesnego wykrycia i wprowadzenia terapii, jest traktowane jako choroba przewlekła, a czas przeżycia pacjentów jest porównywalny do czasu przeżycia ogólnej populacji. Niestety, pomimo bardzo skutecznego leczenia antyretrowirusowego, do tej pory nie udało się nam konwencjonalnymi metodami doprowadzić do eliminacji wirusa z organizmu. Co więcej, nieustanna produkcja nowych cząsteczek HIV, utrata integralności błon śluzowych przewodu pokarmowego i związana z tym ekspozycja na florę jelitową, doprowadzają do stałej aktywacji układu immunologicznego. W efekcie osoby zakażone HIV cechują się zwiększonym ryzykiem wystąpienia m.in. chorób sercowo-naczyniowych i nowotworowych.
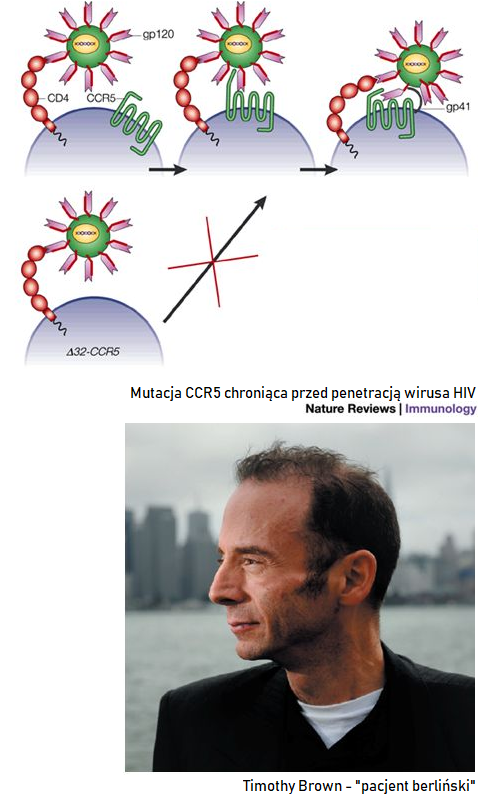
Od czasu kiedy odnotowano pierwsze przypadki AIDS, do chwili obecnej wirusem HIV zakaziło się około 75 mln ludzi na świecie. Pomimo skutecznych metod terapeutycznych do niedawna wiedzieliśmy tylko o jednym przypadku wyleczenia zakażenia dotyczącym Timothy’ego Ray Browna, tzw. “pacjenta berlińskiego”. Chory, z powodu ostrej białaczki szpikowej otrzymał allogeniczny przeszczep szpiku od dawcy będącego nosicielem homozygotycznej mutacji koreceptora CCR5 (CCR5Δ32/Δ32). Tego typu mutacja powoduje, że na powierzchni limfocytytów T nie występuje koreceptor CCR5 (CCR5Δ32/Δ32), wykorzystywany przez HIV (szczep R5) do wniknięcia do wnętrza komórki.
Omawiając przypadek Timothy’ego Browna należy także podkreślić, że w leczeniu schorzenia nowotworowego u „pacjenta berlińskiego” zastosowano napromieniowania całego ciała oraz że wystąpiła u niego reakcja „przeszczep przeciwko gospodarzowi” (GVHD), będąca jednym z najcięższych powikłań po przeszczepie komórek układu krwiotwórczego, kiedy to limfocyty T rozpoznają organizm biorcy jako obcy i zaczynają go atakować. Oba te czynniki mogły mieć wpływ na eradykację wirusa HIV. W 2007 roku po zakończeniu leczenia przeciwnowotworowego odstawiono leki antyretrowirusowe, nie stwierdzając od tej pory replikacji HIV. Pacjent został uznany za wyleczonego.
„Pacjent londyński” – światełko w tunelu?
Z początkiem marca tego roku na łamach Nature pojawiło się doniesienie o prawdopodobnym drugim przypadku wyleczenia z zakażenia HIV, jakie miało dokonać się w Wielkiej Brytanii. Informacje na ten temat zostały również zaprezentowane w trakcie jednej z najważniejszych międzynarodowych konferencji dotyczących terapii antyretrowirusowych - CROI (Conference on Retroviruses and Opportunistic Infections), która odbyła się w tym roku w Seattle.
U pacjenta “londyńskiego”, bo tak szybko został okrzyknięty przez prasę chory, zakażenie HIV zdiagnozowano w 2003 roku. Leczenia antyretrowirusowe rozpoczęto 9 lat później. W roku 2016 doszło u niego do rozwoju ziarnicy złośliwej – nowotworu, który znaczenie częściej występuje w grupie pacjentów zakażonych HIV. Z tego powodu, podobnie jak w casusie “berlińskim”, otrzymał on allogeniczny przeszczep szpiku, również od dawcy będącego nosicielem tej samej homozygotycznej mutacji koreceptora CCR5 (CCR5Δ32/Δ32) – w tym przypadku jedynego wykorzystywanego przez HIV w inwazji na limfocyty T CD4+. Podobnie jak Timothy Brown, również „londyński” chory rozwinął chorobę „przeszczep przeciwko gospodarzowi”. Leczenie antyretrowirusowe zostało w tym przypadku przerwane 16 miesięcy po przeszczepie szpiku.
W chwili obecnej remisja utrzymuje się przez okres 18 miesięcy. Oznacza to, że we krwi pacjenta nie stwierdza się materiału genetycznego wirusa (HIV-RNA), a co ważniejsze naukowcy nie wykrywają również HIV-DNA wbudowanego w limfocytach T CD4+, co przemawia za brakiem wirusa w tzw. miejscach rezerwuarowych, do których należą także komórki ośrodkowego układu nerwowego, narządów płciowych i węzłów chłonnych. To właśnie rezerwuary, w których wirus przebywa w formie nieaktywnej powodują, że dostępnymi lekami oddziaływującymi na różnych etapach namnażania HIV nie jesteśmy go w stanie wyeliminować z organizmu pacjentów. Stwierdzono także spadek przeciwciał dla wirusa HIV-1, podobny do tego obserwowanego u pacjenta „berlińskiego”.
Obecnie jest jeszcze za wcześnie by można z całą pewnością stwierdzić, że mamy do czynienia z przypadkiem ponownego wyleczenia z zakażenia HIV, a nie tylko z chwilową remisją. Należy również podkreślić, że tego typu terapia nie jest metodą, która mogłaby znaleźć powszechne zastosowanie w grupie pacjentów skutecznie do tej pory leczonych antyretrowirusowo, a u których nie doszło do rozwoju powikłań nowotworowych. Przeszczep szpiku wiąże się ze zbyt dużym ryzkiem wystąpienia ciężkich powikłań i jest terapią bardzo kosztowną.
Niemniej jednak jest to niewątpliwie kolejny przełom, dający naukowcom wskazówki do dalszym poszukiwań interwencji terapeutycznych, które miałyby na celu eliminację wirusa z organizmu i trwałe wyleczenie zakażenia HIV. Wreszcie, jest to także ogromna nadzieja dla milionów osób żyjących z HIV na całym świecie, bo pomimo ogromnego postępu AIDS wciąż nie tylko choroba przewlekła związana z ryzkiem wystąpieniem licznych powikłań, w tym także schorzeń nowotworowych, ale także taka, która wiąże się z ryzykiem stygmatyzacji i brakiem akceptacji społecznej.
dr hab. Monika Bociąga-Jasik
Piśmiennictwo:
- Gupta R.K. et al.: HIV-1 remission following CCR5Δ32/Δ32 haematopoietic stem-cell transplantation. Nature 2019, March 5 (Epub ahead of print)
- Cohen J.: Has a second person with HIV be cured? Science 2019, 363, 1021.
- Mitchell B.I. et al.: Impact of Meyeloid Reservoirs in HIV Cure trials. Curr HIV/AIDS Rep. 2019, March 5 (Epub ahead of print)
Zdjęcie w tekście: Zhaolin Hua, Institute of Biophysics of Chinese Academy of Sciences
--------------------------------------------------------------------
Ciekawe? Przeczytaj także:




