 Widok zawartości stron
Widok zawartości stron
 Widok zawartości stron
Widok zawartości stron
 Widok zawartości stron
Widok zawartości stron
Molekularna blokada
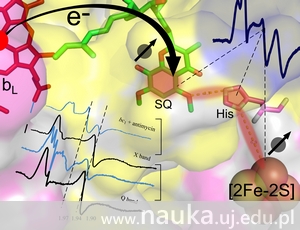
Naukowcy z UJ pokazują jak istotne dla przekazywania energii białka są zabezpieczone przed niekorzystnymi reakcjami ubocznymi. Odkryty mechanizm funkcjonuje zarówno w komórkach zwierzęcych, jak i roślinnych.
![]() Więcej o nauce?! Dołącz do profilu strony. www NAUKA.uj.edu.pl na Facebooku
Więcej o nauce?! Dołącz do profilu strony. www NAUKA.uj.edu.pl na Facebooku
Jak to działa?
Takie funkcjonowanie wspomnianych białek jest możliwe dzięki reakcjom przekazywania elektronu pomiędzy kolejnymi elementami złożonego łańcucha białkowego. W żywej komórce warunki nieustannie się zmieniają, a przez to i tempo przepływu elektronu przez łańcuchy powinno być odpowiednio dostosowane. Niebezpieczne mogą być zwłaszcza momenty przestoju (np. gdy zapotrzebowanie na energię raptownie maleje), w których to elektrony mogłyby angażować się w reakcje uboczne, niekorzystne energetycznie, a nawet szkodliwe, tak jak powstawanie wolnych rodników w reakcji przeniesienia pojedynczego elektronu na tlen.
 Przy użyciu zaawansowanych technik spektroskopowych badacze z UJ, wykryli nowy stan molekularny, który w sytuacji takiego „spowolnienia”, przytrzymuje elektron w bezpiecznej formie, niewchodzącej w reakcje z tlenem. Taki stan może trwać nawet parę sekund, co w porównaniu z innymi mikro- i millisekudowymi reakcjami oznacza bardzo długi czas. Jednocześnie elektron w tym stanie pozostaje w „gotowości” do „przeskoczenia” na kolejne elementy łańcucha, gdy tylko ten zostanie „odblokowany”.
Przy użyciu zaawansowanych technik spektroskopowych badacze z UJ, wykryli nowy stan molekularny, który w sytuacji takiego „spowolnienia”, przytrzymuje elektron w bezpiecznej formie, niewchodzącej w reakcje z tlenem. Taki stan może trwać nawet parę sekund, co w porównaniu z innymi mikro- i millisekudowymi reakcjami oznacza bardzo długi czas. Jednocześnie elektron w tym stanie pozostaje w „gotowości” do „przeskoczenia” na kolejne elementy łańcucha, gdy tylko ten zostanie „odblokowany”.
Praca opublikowana w PNAS pokazuje, że opisywany, metastabilny stan występuje zarówno w komórkach zwierzęcych, jak i roślinnych. Okazuje się, iż w tych ostatnich pojawia się znacznie częściej, co może być powiązane z faktem, że w komórkach roślinnych stężenie tlenu jest wyższe. Takiej sytuacji nie przewidywał żaden z modeli działania, proponowany dotychczas dla tej grupy białek.
Naukowcy pokazują w ten sposób możliwy mechanizm, który zabezpiecza białka przed szkodliwymi reakcjami ubocznymi, które mogąc zajść w warunkach dostępu do tlenu. Pokazuje ona też ten element mechanizmu, który może przyczyniać się do tego, że działają one ze zdumiewająco wysoką sprawnością.
Autorami pracy w PNAS są Marcin Sarewicz, Łukasz Bujnowicz (wspólne pierwsze autorstwo) i Artur Osyczka (autor korespondencyjny) – wszyscy z Zakładu Biofizyki Molekularnej Wydziału Biochemii, Biofizyki i Biotechnologii UJ, oraz Satarupa Bhaduri, Sandeep K. Singh i William A. Cramer z Purdue University w Stanach Zjednoczonych.


![Pszczoły na diecie? [wideo]](/documents/74541952/147053668/bee2_230x300.png/132b8ed5-2598-4f5d-a105-c565636e3911?t=1616428310238)